Il Dispositivo Medico (DM) , strumento per raggiungere obiettivi di efficienza e sostenibilità del sistema
PRIMO PIANOREPORTSSOSTENIBILITA 16 Giugno 2020 digitalvoice

Di questo si è parlato durante il WEBINAR ‘FOCUS HTA E DISPOSITIVI’, organizzato da Motore Sanità, in collaborazione con Officina Motore Sanità, con il patrocinio di AReSS PUGLIA, Ospedale Policlinico San Martino, Rete Oncologica Veneta e SIHTA – Società Italiana di Health Technology Assessment e con il contributo incondizionato di Amgen, Chiesi, Merck, Mylan e Teva.
Il settore dei Dispositivi Medici (DM) impatta fortemente sullo sviluppo tecnologico, scientifico e produttivo del nostro Paese, contribuendo al miglioramento della salute, efficienza e sostenibilità del SSN e del sistema sociosanitario. Individuare regole e strumenti per la valutazione dei DM deve essere obiettivo prioritario per il comparto salute, delle Istituzioni Politiche, delle Istituzioni Sociali e Previdenziali (INPS, INAIL), medici e pazienti. L’Italia è ancora indietro nonostante ci siano strumenti da implementare come il Piano Nazionale HTA, l’It.DRG (progetto per tracciare dispositivi medici all’interno dei dati amministrativi) e il Codice Appalti (dove bisognerebbe prediligere l’affidamento del DM e superare la mera logica del prezzo, ma che ancor oggi, spesso, si continua a preferire,così da inficiare una valorizzazione corretta del device medico).
“Esistono metodologie e strumenti per misurare, valutare, finanziare, fare ricerca sui dispositivi, manca però la fase implementativa, per far sì che i dispositivi vengano correttamente valorizzati così da garantire un rapido accesso ed utilizzo degli stessi. Non si può parlare di sanità e finanziamento basati sul valore se non misuriamo il reale valore delle tecnologie. Per farlo servono ricerca e dati, che non possono essere misurati senza codici per tracciare l’attività e fare benchmarking. Bisogna investire in una moderna infrastruttura informatica, con competenze e assetto organizzativo di responsabilità, ma perché tutto ciò accada è culturale il primo passo da fare: concepire il dispositivo medico come un investimento”, ha spiegato Francesco Saverio Mennini, Research Director-Economic Evaluation and HTA, CEIS,Università degli Studi di Roma “Tor Vergata”.
“L’HTA è un processo che usa metodi espliciti per determinare il valore di una tecnologia sanitaria in tutto il suo ciclo di vita. L’obiettivo è informare le decisioni alla promozione di sistemi sanitari equi, efficienti e di alta qualità (INAHTA, 2020). La tecnologia sanitaria è un intervento di prevenzione, diagnosi, terapia, riabilitazione e promozione della salute: può trattarsi di un test, un dispositivo, un farmaco, un vaccino, una procedura, un programma o un sistema. Il processo valutativo deve essere formale, sistematico e trasparente e riguarda per lo più l’efficacia, la sicurezza, i costi e l’impatto economico, gli aspetti etici, sociali, culturali, giuridici, organizzativi ed ambientali, dal punto di vista di tutti gli stakeholder. Esso può essere applicato in tutte le fasi del ciclo di vita della tecnologia sanitaria: per esempio, nel pre-market, nella fase regolatoria, nel post-market, nel disinvestimento”, ha detto Carlo Favaretti, Presidente onorario Società Italiana di Health Technology Assessment
“Con il Covid19 abbiamo visto l’errore strategico nel non aver rafforzato l’assistenza territoriale, la medicina generale è disponile ad interagire per una tecnologia di primo livello per poter dare una risposta al cittadino, l’HTA può dare indicazioni importanti su quali modelli utilizzare”, ha aggiunto Massimo Magi, Segretario FIMMG Marche e Presidente Fondazione Nusa e Nusa Servizi
In Italia sono stati registrati oltre un milione di modelli di dispositivi medici e oltre 45mila dispositivi medico-diagnostici in vitro. Una varietà infinita di prodotti che va dalle più avanzate apparecchiature per le TAC ai guanti di lattice usa e getta, infatti viene definito dal Ministero della Salute ‘dispositivo medico’ qualsiasi strumento, apparecchio, impianto, sostanza o altro prodotto, utilizzato da solo o in combinazione (compreso il software informatico impiegato per il corretto funzionamento) e destinato dal fabbricante ad essere impiegato nell’uomo a scopo di diagnosi, prevenzione, controllo, terapia o attenuazione di una malattia; di diagnosi, controllo, terapia, attenuazione o compensazione di una ferita o di un handicap; di studio, sostituzione o modifica dell’anatomia o di un processo fisiologico; di intervento sul concepimento, il quale prodotto non eserciti l’azione principale, nel o sul corpo umano, cui è destinato, con mezzi farmacologici o immunologici né mediante processo metabolico ma la cui funzione possa essere coadiuvata da tali mezzi.
Spesa sostenuta: quasi 6 miliardi
I costi sostenuti nel 2017 (ultimi dati disponibili) dal Servizio Sanitario Nazionale per l’acquisto di dispositivi medici ammontano a quasi 5.992 milioni di euro secondo i dati del Conto economico degli enti del Servizio Sanitario Nazionale, e sono così divisi:
- dispositivi medici 4.115 milioni
- dispositivi medici impiantabili attivi 524 milioni
- dispositivi medico-diagnostici in vitro 1.351 milioni
In Italia 3,957 imprese e 76 mila dipendenti
Secondo i dati forniti da Confindustria il settore dei dispositivi medici in Italia genera un mercato che vale 16,5 miliardi di euro tra export e mercato interno e conta 3.957 aziende, che occupano 76.400 dipendenti. Si tratta di un tessuto industriale molto eterogeneo, altamente innovativo e specializzato, dove le piccole aziende convivono con i grandi gruppi. In Italia il mercato delle imprese del settore è rivolto per il 66% verso il Servizio Sanitario Nazionale e rappresenta il 7,4% della spesa totale, che corrisponde a circa 190 € pro-capite, valore inferiore alla media dei principali paesi europei.
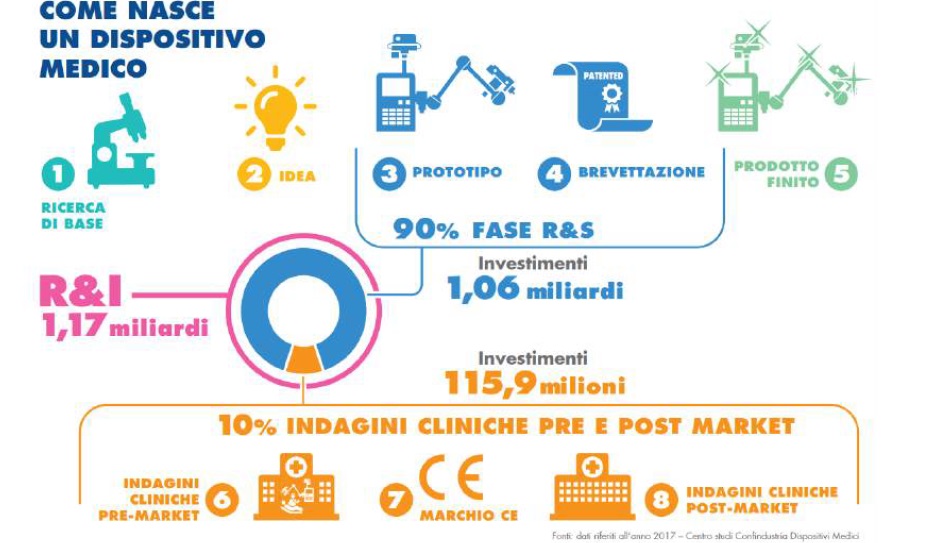
Come nasce un dispositivo medico?
Il processo di nascita di un dispositivo medico dalla ricerca di base alla sua immissione in commercio fino alle indagini cliniche è altamente innovativo e richiede importanti investimenti.
Come valutare le nuove tecnologie?
Tradizionalmente, la valutazione delle tecnologie sanitarie rappresenta il ponte tra il mondo tecnico-scientifico e quello dei decisori. Ma la valutazione delle tecnologie sanitarie è anche un’occasione strutturata di incontro tra le diverse esigenze e aspettative di tutte le parti interessate all’assistenza sanitaria, che ne consente il successivo bilanciamento su criteri espliciti e condivisi tra le parti stesse. È il contesto nel quale i decisori politici, chi ha responsabilità organizzative, i professionisti, i pazienti e i fornitori contribuiscono al processo decisionale (cosa fare, come fare, quando fare, se fare…) e rispondono reciprocamente di tali decisioni.
Il sistema di valutazione HTA
La valutazione delle tecnologie sanitarie (Health Technology Assessment – HTA) è un processo multidisciplinare che sintetizza le informazioni sulle questioni cliniche, economiche, sociali ed etiche connesse all’uso di una tecnologia sanitaria, in modo sistematico, trasparente, imparziale e solido. Il suo obiettivo è contribuire all’individuazione di politiche sanitarie sicure, efficaci, incentrate sui pazienti e mirate a conseguire il miglior valore. Il processo di HTA si basa su evidenze scientifiche tratte da studi, che vengono considerate per specifiche tipologie di intervento sanitario su determinate popolazioni di pazienti, confrontando gli esiti e i risultati con quelli di tecnologie sanitarie di altro genere o con lo standard di cura corrente. Affinché l’HTA sia funzionale alla governance dei dispositivi medici e alla programmazione degli investimenti occorre orientare la valutazione verso le tecnologie di maggior interesse, ovvero quelle innovative, quelle ad elevato impatto clinico, economico, organizzativo ed assistenziale, o che presentano elevati rischi per i pazienti o per le quali si rilevano particolari possibilità di utilizzo inappropriato.
Il Webinar è andato in onda su www.motoresanita.it
Nella foto Francesco Saverio Mennini, Research Director-Economic Evaluation and HTA, CEIS,Università degli Studi di Roma “Tor Vergata”



















